
2024年1月,士泽生物医药(苏州/上海)有限公司(Roche Accelerator Member;以下简称“士泽生物”)临床级自体iPSC衍生多巴胺能神经前体细胞注射液经颅内立体定位注射微创手术方式移植治疗帕金森病在上海市东方医院(同济大学附属东方医院)(以下简称”东方医院“)成功完成:为中国首例临床级iPS衍生细胞移植治疗帕金森病,也是全中国首例、全世界第二例自体iPS衍生细胞替代性移植治疗帕金森病(推荐阅读:花费1400万,他雇佣顶尖团队给自己做了这台世界首例移植术)
此次士泽生物与合作医院完成的全中国首例、全世界第二例临床级自体iPS衍生细胞治疗帕金森病的神经外科微创手术移植在两小时以内完成:首例受试者接受临床级iPS衍生细胞移植后,无手术及围术期的并发症或其他不良安全事件,各项检测指标正常且已顺利出院,平稳度过观察期并进入正式随访期。


帕金森病(Parkinson's disease,PD)是全球第二大神经退行性疾病,我国是全球帕金森病第一大国,帕金森病主要致病原因为中脑黑质区多巴胺能神经元发生了退行性病变和死亡,进而引起震颤、运动迟缓、肢体僵硬、步态异常等运动功能的逐步退化,直至病人死亡。我国65岁以上人群中,帕金森病发病率约为1.7%,预计至2030年,我国帕金森病患者人数将达到500万左右,现有的传统药物治疗或手术治疗不能再生多巴胺能神经元或解决神经元退行性病变和死亡的问题,尚不能改变帕金森病的疾病发展进程。

士泽生物创始人李翔博士表示:
士泽生物此次顺利完成的临床给药:为中国首例临床级iPS衍生细胞移植治疗帕金森病,也是全中国首例、全世界第二例个性化自体iPS衍生细胞替代性移植治疗帕金森病,为中国iPS衍生细胞治疗帕金森病留下了中国“首个及首例”的行业记忆!
士泽生物此次开展的临床研究项目由国家卫生健康委员会和国家药品监督管理局正式批准开展:是我国首个iPS衍生细胞治疗帕金森病的国家级备案干细胞临床研究项目,也是我国迄今为止唯一一个获得国家两委局正式批准开展的iPS衍生细胞治疗神经系统疾病的国家级临床研究项目。
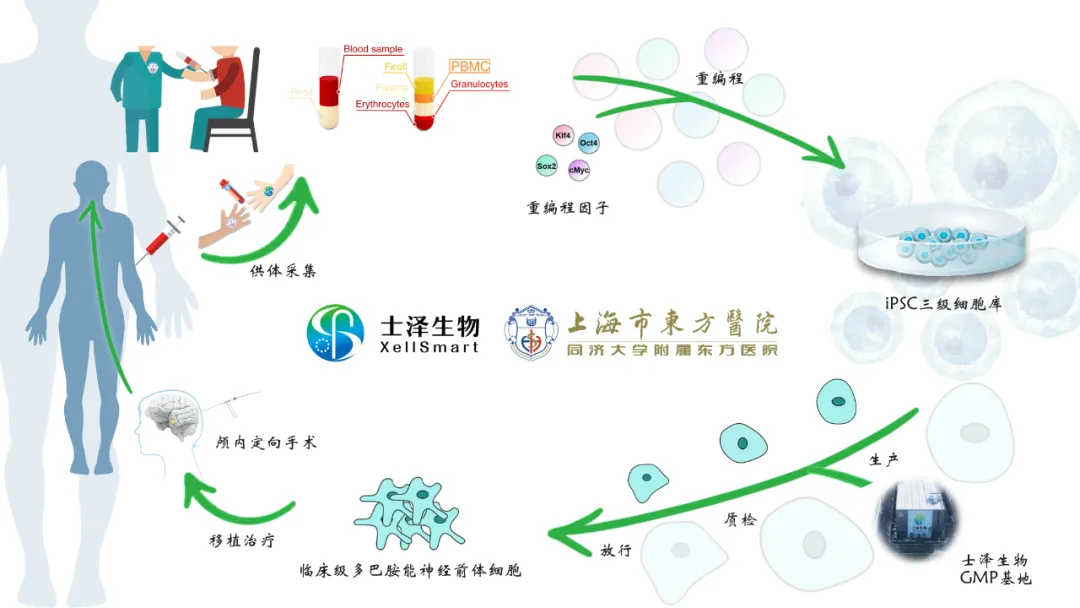
士泽生物获得两委局正式批准开展中国首个临床研究及已经顺利完成个性化自体iPS衍生多巴胺能神经前体细胞的临床级注射液的生产、质检、放行及与合作医院完成的临床微创移植,是对士泽生物自主运营和已经建立的临床级iPS衍生细胞注射液治疗帕金森病的整体产品及管理体系,和GMP规范下的临床级iPS衍生细胞的“生产-制备-放行”的一站式平台能力的重要验证和论证。
相对美国已经完成全世界第一例的实验室级别自体iPS衍生细胞移植治疗帕金森病,中国士泽生物自研及国产的临床级iPS衍生细胞注射液,具有多方面的显著对比优势,其中,士泽生物的治疗成本不及美国同类治疗成本的三十分之一,对追求个性化治疗帕金森病有实质需求的中国及全球帕金森病患者更加经济可及,具有明确的市场化竞争优势(推荐阅读:花费1400万,他雇佣顶尖团队给自己做了这台世界首例移植术)
自士泽生物在合作医院发起临床招募以来,全国帕金森病患者报名意愿强烈,更加凸显出作为全世界帕金森病第一大国,中重度帕金森病未被满足的重大临床刚需。士泽生物团队将严格遵守医学及伦理要求,与合作医院临床及管理团队一起,以科学严谨的态度推进后续国家级干细胞备案临床研究工作,不忘初心,不懈进取:
期待最终能够为帕金森病患者开发出安全、有效、可控及经济可及的,或实现高价值个性化医疗的,具有实质临床获益的细胞药物和解决方案!
士泽生物团队全身心All In,低调实干,行胜于言,持续不断的以实际事实和结果为证!
国“士”无双的干细胞创新药物,
福“泽”千万受苦难的病患家庭!
帕金森病受试者招募
关于士泽生物
士泽生物创始人李翔博士专注iPS衍生细胞创新药的科学研发及产业化十五年,士泽生物长期专注于开发临床级iPS衍生细胞药治疗帕金森病等尚无实质临床解决方案的神经系统疾病:
士泽生物组建了具有国际竞争力及产业界背景的全职团队,士泽生物核心团队成员来自北京大学、清华大学、复旦大学、上海交通大学、同济大学、中国科学院及美国威斯康星大学、霍普金斯大学等海内外著名高校或细胞治疗业界知名公司,团队拥有国际及产业界最前沿的干细胞治疗技术和转化经验。
士泽生物已运营>5000平方米的研发中心、B+A级GMP基地及质控中心,iPS衍生细胞药的主要研发管线已完成核心CMC开发、建立了全流程的临床级制备工艺及质量控制体系,并完成多种临床级iPS衍生亚型特化神经前体细胞治疗产品的正式试生产。
士泽生物临床级iPS衍生多巴胺神经前体细胞治疗帕金森病的首发管线:
由国家卫生健康委员会与国家药品监督管理局( 简称两委)正式批准开展临床研究,是我国首个经国家两委局正式批准的iPS衍生细胞治疗帕金森病的国家级临床研究,也是我国迄今为止唯一一个正式获批的iPS衍生细胞治疗神经系统疾病的国家级干细胞备案临床研究项目(【国内首个】士泽生物iPSC衍生细胞治疗帕金森病获批国家临床级备案临床研究)。
士泽生物已完成的中国首例临床级iPS衍生细胞药移植治疗帕金森病,为全中国首例、全世界第二例个性化自体iPS衍生细胞代替性移植治疗帕金森病。
士泽生物从数百家医药企业中脱颖而出,正式入选成为Roche Accelerator在中国的十五家合作成员企业之一。士泽生物正在罗氏体系提供的全球专业顾问团队及配套科学资源的合作支持下,加速推动士泽生物 iPS 衍生细胞治疗帕金森病新药管线的研发和产业化,并入选国家生物药技术创新中心细胞疗法“重点攻关项目”。
士泽生物建立了一批具有自主知识产权、国际领先的新技术、新平台,能够为可持续输出自研创新管线提供关键保障:
2023年,士泽生物自研的全球首发研发管线临床级iPS衍生亚型神经前体细胞治疗渐冻症,获得美国FDA认证授予孤儿药资格并享有获批上市后7年市场独占权等,为中国首个自研和国产iPS衍生细胞药获得FDA认证并授予全球孤儿药资格。
基于士泽生物已开发的针对渐冻症的全球首发iPS衍生细胞孤儿药,士泽生物首先与国内头部医院合作并且已正式启动针对散发型渐冻症患者的临床研究、及针对特定突变型的基因修正自体iPS衍生细胞治疗渐冻症的前沿临床研究,均为全球首发及首个临床研究(FIC)。
自李翔博士全职创立士泽生物以来,已完成由峰瑞资本、启明创投、礼来亚洲基金、红杉中国等著名风险投资机构领投的多轮数亿元融资。2022至2023年,在新冠及医药领域整体寒冬的大环境下,李翔博士带领士泽生物完成了由启明创投、礼来亚洲基金、金圆展鸿、中新资本共同领投,元禾控股、北京大学科技成果转化基金、钧山资本、阿里健康和华泰紫金等新股东联合投资的逾两亿元A轮融资及A+轮追加融资。